Ejemplo de Energía de Enlace Químico
En los enlaces químicos de una molécula, las fuerzas eléctricas atractivas son las que hacen que existan los estados de ligamientos. Es decir, los átomos de la molécula no pueden escapar de ella sin un aporte de energía externa. Los estados de enlaces comparados con los átomos libres, implican una energía potencial negativa, por lo que cualquier enlace químico, tiene asociado una energía potencial negativa. Se puede usar el principio de conservación de la energía, como una herramienta de análisis general para la búsqueda de reacciones químicas que impliquen cambios en los enlaces.
Considérese la combinación de dos moléculas de H2 con una molécula de O2 para formar dos moléculas de agua, H2O. Energéticamente, se puede considerar que el proceso necesita energía para disociar el H2 y el O2, pero luego el ligamiento del H2O retorna el sistema a un estado de ligamiento con potencial negativo. Realmente es mas negativo que los estados ligados de los reactivos, y la formación de dos moléculas de agua, libera realmente 5,7 electron voltios de energía.
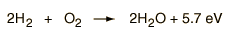
El balance de energía antes y despues de la reacción, se puede ilustrar esquemáticamente con el estado en el cual todos los átomos están libres -tomados estos como referencias de energías-.

Si se midieran las energías de disociación del H2 y el O2 y la liberación de energía en su reacción, ofrecerían una ruta experimental para la determinación de la energía de enlace total de la molécula de H2O.
El método de balance de energía también puede ser útil en el análisis de un enlace iónico.
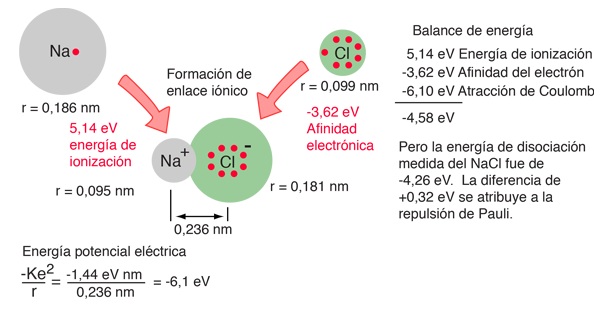
Los parámetros experimentales disponibles de la conservación de la energía para el sodio, el cloro y la molécula de NaCl, proporcionan los datos para el cálculo de la energía de disociación de la molécula. Los pasos para la formación de la molécula iónica del NaCl podrían considerarse como (1) proporcionar la energía de ionización de 5,14 eV para ionizar el Na, luego,(2) la recuperación de -3,62 eV de la afinidad electrónica del Cl. Luego, basadas en la longitud de enlace conocida de 0,236 nm, la energía de enlace de las fuerzas de atracción eléctricas. Pero este proceso no está de acuerdo con la medida de la energía de disociación del NaCl, de 4,26 eV. Esto revela la presencia de otro término de energía repulsiva llamado la repulsión de Pauli (+0,32 eV).
| Enlaces Químicos |
| HyperPhysics*****Física Cuántica*****Química | M Olmo R Nave |